ムコ多糖症Ⅱ型の治療

ムコ多糖症(mucopolysaccharidosis:MPS)は、グリコサミノグリカン(GAG)を段階的に分解するライソゾーム酵素の欠損により発症する先天代謝異常症である。酵素補充療法や造血幹細胞移植により治療可能な疾患であるが、病状の進行を抑制するためには早期の診断と治療開始が望まれる。
疾患の概念
ムコ多糖症は、細胞内に蓄積するグリコサミノグリカンによって特徴的な顔貌や関節拘縮、肝・脾腫大、病型によっては精神発達遅延などの中枢神経症状をきたす全身性の疾患である。ムコ多糖症は、蓄積されるグリコサミノグリカンの種類、臨床症状から7タイプの病型に分類され、これまでに11種類の欠損酵素が知られている。
ムコ多糖症全体の発症頻度は、出生5万人に1人程度と推定されている。わが国ではムコ多糖症Ⅱ型(ハンター症候群)が全体の約半数を占め、次いでムコ多糖症Ⅲ型が約17%、ムコ多糖症Ⅰ型が約15%、Ⅳ型が約10%の頻度である。
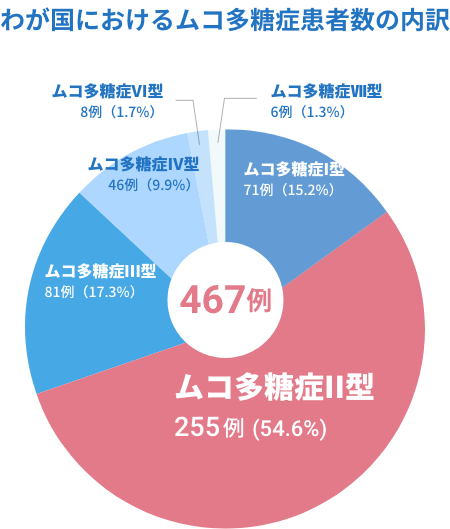
鈴木康之. ムコ多糖症の疫学. 折居忠夫ほか編. ムコ多糖症UPDATE.
イーエヌメディックス; 2011. P.7-8.
診断の契機となる症状、所見
ムコ多糖症は症状が多彩であるため、幅広い診療科を受診する機会があるが、特徴的な症状からムコ多糖症を疑うことができれば、早期診断は可能である。
受診する契機となる症状としては、鼠径・臍ヘルニア、発達の遅れ、とくに言葉の遅れや多動、頭囲拡大や骨・関節の変形、繰り返す中耳炎、心雑音、肝腫大などである(表)。また、紹介元は小児科が最も多いが、それ以外にも耳鼻科や整形外科などもある。
耳鼻科領域では、繰り返す中耳炎が一つの診断の契機となる症状である。また、患者家族会へのアンケート調査では、2~3歳ころの“言葉の遅れ”が医療機関を受診するきっかけとして最も多かった。
ムコ多糖症の主な特徴的症状
特徴的顔貌(ムクムクした顔貌、巨舌など)
反復性中耳炎、難聴
椎骨の変形、関節拘縮
ヘルニア(鼠径・臍)、肝腫大
心雑音(心臓弁膜症)
精神発達遅延(言葉の遅れなど)
治療方針の決定
ムコ多糖症を疑えば全身の骨の単純X線検査を行い、尿中ウロン酸分析で蓄積するグリコサミノグリカンを特定する。
さらに、血液あるいは一部の組織を採取し、病型別で欠損する酵素活性を測定することにより確定診断を行う。
また、遺伝子検査では、疾患の重症度や治療法の選択において有益な情報が得られる場合がある。確定診断後、治療法として病型、重症度から酵素補充療法あるいは造血幹細胞移植が選択される。
治療の実際
ムコ多糖症は、酵素補充療法や造血幹細胞移植により治療可能な疾患である。
酵素補充療法
酵素補充療法は、遺伝子組換え技術によって合成された酵素製剤を、点滴静注などにより体外から補充する治療法であり、わが国ではムコ多糖症Ⅰ型、Ⅱ型、ⅣA型、Ⅵ型に対する酵素補充療法が実用化されている(2022年8月現在)。酵素補充療法は安全性が高く、治療効果についても十分なエビデンスが蓄積されており、海外のレジストリー研究では生存期間、生命予後の10年程度の延長が報告されている薬剤もある。
酵素補充療法開始のタイミングは、可能な限り早期に開始することが重要である。乳幼児期より酵素補充療法を開始できる症例では、症状が出現してから治療を開始する症例に比べて、顔貌の変化や関節症状の進行を遅らせることができる可能性がある。
酵素補充療法の開始早々(6ヵ月~1年以内)に粘膜や皮膚の肥厚が軽減する。皮膚が柔らかく感じられるなどの効果は、酵素補充療法の治療開始早々にみられる。
その結果…
- 関節の周囲の結合織も柔らかくなり、可動域も改善する。
- 特徴的な顔貌や巨舌も目立たなくなる。
- 繰り返す中耳炎の頻度が少なくなる。
- 上気道の粘膜肥厚の軽減により、いびきや睡眠時無呼吸の改善もみられる。
また、酵素補充療法により、肝腫大が急速に改善するなど、血流が豊富な臓器には高い効果を示すことが知られている。
その一方で、精神運動発達遅滞や神経学的退行を改善することは期待できない。これは、血液脳関門の存在により、高分子である酵素が血管から脳実質内に移行できないためである。
近年、脳室内投与の酵素製剤や血液脳関門を通過することのできる技術を用いた酵素製剤の登場により、ムコ多糖症Ⅱ型の中枢神経症状に対してより有効な治療が選択できるようになった。いずれも、メカニズムとして中枢神経症状の改善が確認され、早期に投与することでより良好な効果が期待されている。
造血幹細胞移植
造血幹細胞移植は、酵素補充療法が開発される以前から主に重症型ムコ多糖症に対して、適切な移植ドナーが見つかった場合に行われてきた。
近年、医療技術の進歩とともに造血幹細胞移植における安全性も高まってきている。生着すれば通院回数を減らすことができるなど、患者にとってメリットも大きい。
但し、移植ドナーが保因者の場合は、血中の酵素活性が約半分と少ない。
とくにX連鎖性劣性遺伝形式をとるムコ多糖症Ⅱ型においては、ドナーが女性保因者であった場合、X染色体のランダムな不活性化現象があるため、症例によっては酵素活性がほぼゼロになっていることもあるので、ドナーの選択には十分な注意が必要である。
合併症に対する治療、対症療法
最も注意が必要なのが整形外科的な合併症である。
頚髄部分は生理的に隙間が狭いため、頚椎症として神経症状を呈する危険性が高い。整形外科と連携して診察や定期的な画像検査などを行い、観察を続ける必要がある。
また、滲出性中耳炎が重症化した場合には、鼓膜チューブ留置術が必要となる頻度も高い。弁膜症は成人では弁置換術などの手術が必要になるケースもある。幸いにも小児期では手術が必要なケースは少ないが、病変が消失することはなく、注意深い観察が必要である。
日常生活についての注意点
症状の程度にもよるが、頸椎の動きの制限があることから、日常生活では頸部に負荷がかからないように注意する必要がある。
また、中枢神経症状の進行例では水頭症を発症することがあるので、急な知的レベルや意識レベルの低下にも十分に注意しなければならない。
さらに、手首にムコ多糖が蓄積して神経を圧迫することによって生じる手の痺れや母指球の萎縮(手根管症候群)によるQOL(Quality of Life)の低下、弁膜症による階段を上る際の息苦しさなど、病状の進行に伴ってさまざまな症状が現れてくることから、これら予想される合併症の症状を詳細に伝えて注意を促すことが重要である。
新たな治療アプローチ
今後、ムコ多糖症に対するより良い治療法の開発も進められている。遺伝子治療は非常に期待される治療であり、脳に直接欠損酵素の遺伝子ベクターを投与する方法、自分の骨髄に必要な遺伝子を導入する方法などが検討されている。また、mRNA医薬品も有望だと考えられる。しかし、いかに優れた治療法が開発されたとしても、発症前あるいは発症早期に治療を開始しないと良好な治療効果は期待できないことに留意すべきである。

ドクターズコラムはこちら
